Enlace covalente 2011
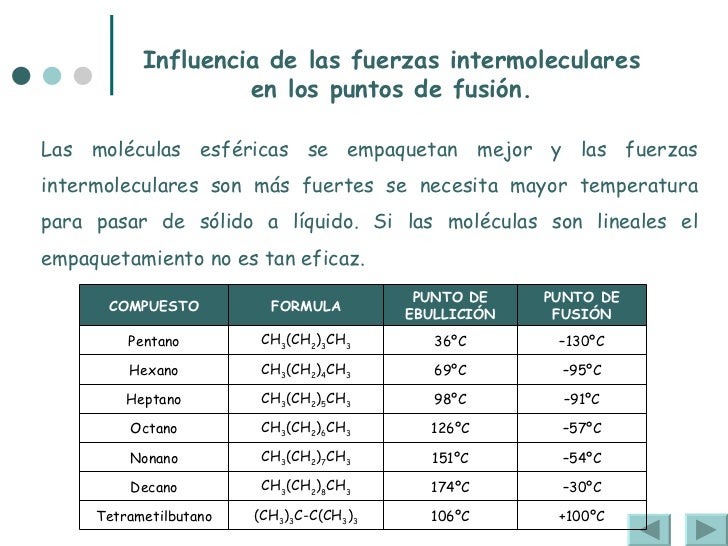
Enlace iónico. Representación de la unión iónica entre el litio y el flúor para formar el fluoruro de litio. El litio tiene una energía de ionización baja y cede fácilmente su único electrón de valencia a un átomo de flúor, que tiene una afinidad positiva con los electrones y acepta el electrón donado por el átomo de litio.
PPT punto de ebullición PowerPoint Presentation, free download ID3116840

Los compuestos iónicos tienen características muy particulares, como puntos de fusión y ebullición altos,. Formación del Enlace Iónico. La formación de un enlace iónico ocurre entre átomos con diferencias significativas en electronegatividad, mayor o igual a 1,7 según la escala de Pauling. En términos generales, los metales.
7 propiedades del ENLACE iónico resumen fácil!

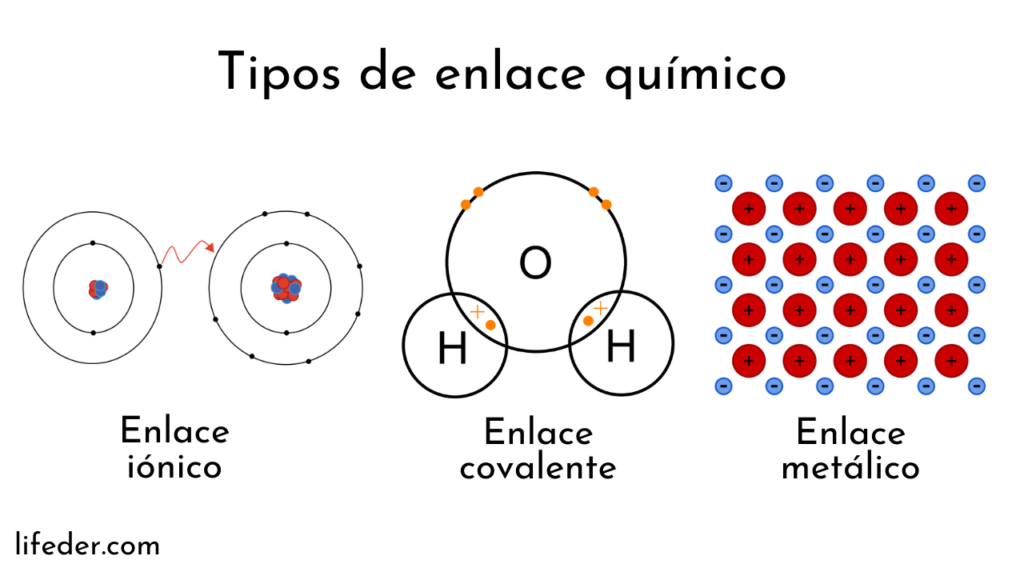
El enlace covalente se forma entre 2 átomos no-metálicos que tienen electronegatividad similar. Ninguno es los suficientemente "fuerte" para atraer electrones del otro. Para estabilización, comparten electrones de su órbite molecular más externa. El enlace iónico se forma entre un átomo metálico y uno no-metálico.
Punto de fusión y ebullición (1) [PPTX Powerpoint]

Otra propiedad característica de los compuestos iónicos es su conductividad eléctrica. La siguiente figura muestra tres experimentos en los que dos electrodos que están conectados a una bombilla se colocan en vasos de precipitados que contienen tres sustancias diferentes. Figura 8.9.3 8.9. 3: (A) El agua destilada no conduce electricidad.
Ejemplos De Enlaces Ionicos En La Vida Cotidiana Compartir Ejemplos

1 El punto de ebullición en el enlace iónico: fundamentos y aplicaciones en química y biología. 1.1 ¿Cómo influye la fuerza del enlace iónico en el punto de ebullición de un compuesto? 1.2 ¿Qué factores determinan el punto de ebullición en los compuestos con enlaces iónicos?
Enlace químico. Tipos, características y ejemplos

El enlace iónico se forma entre átomos con diferencias significativas en electronegatividad, lo que da como resultado la formación de iones positivos y negativos. Los compuestos iónicos tienden a tener puntos de fusión y ebullición altos debido a las fuertes fuerzas electrostáticas entre los iones. Este fenómeno se debe a la necesidad.
Enlace iónico características, cómo se forma y ejemplos
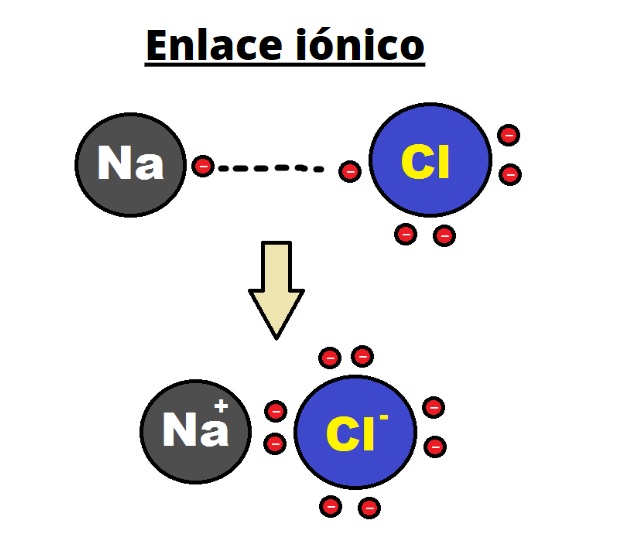
Suelen cristalizarse: debido a la estructura tridimensional de un enlace iónico, estos favorecen redes cristalizadas frágiles. Altos puntos de ebullición y fusión (300º C a 1000º C): ya que existe una fuerza de atracción muy potente entre los iones, estos deben someterse a altos puntos de fusión o ebullición para modificar su estado.
ELECTRONEGATIVIDAD Y TIPOS DE ENLACE IÓNICO Y COVALENTE Curso para la UNAM

Nuestra misión es mejorar el acceso a la educación y el aprendizaje para todos. OpenStax forma parte de Rice University, una organización sin fines de lucro 501 (c) (3). Done hoy y ayúdenos a llegar a más estudiantes. Este libro de texto gratis es un recurso de OpenStax escrito para mejorar el acceso que tienen los estudiantes a materiales.
Enlace iónico qué es, características, propiedades y ejemplos
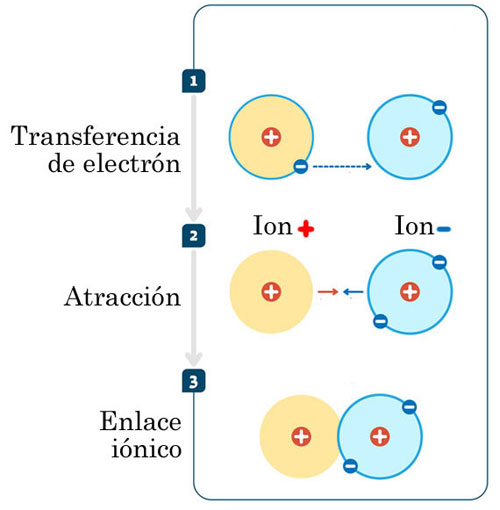
Tienen altos puntos de fusión y de ebullición.. El enlace iónico sucede cuando se da una unión de dos átomos por medio del enlace iónico, que sucede cuando un electrón abandona el átomo que tiene menor carga electronegativa y pasa a formar parte de la nube electrónica del átomo que es más electronegativo. Los enlaces iónicos se.
Tema 6 ENLACE QUIMICO
Aprende gratuitamente sobre matemáticas, arte, programación, economía, física, química, biología, medicina, finanzas, historia y más. Khan Academy es una organización sin fines de lucro, con la misión de proveer una educación gratuita de clase mundial, para cualquier persona en cualquier lugar.
10 Ejemplos De Enlaces Ionicos Y Covalentes Opciones de Ejemplo

Enlace iónico (diferencia entre 1.7 y 3.3 ) Un enlace iónico se forma cuando los electrones se transfieren completamente de un átomo a otro. Durante este proceso, un átomo pierde electrones y otro los gana, formándose iones. Este fenómeno se presenta entre átomos con diferencias de electronegatividad muy alta (superior o igual a 1.7), el átomo más electronegativo atrae con mayor.
🌡 Puntos de Fusión y Ebullición 🔥 ¿Qué son? EJEMPLOS [Fácil y Rápido] FÍSICA QUÍMICA YouTube

Ejemplos de enlace iónico. Fluoruros (F-). Aniones que forman parte de sales obtenidas a partir del ácido fluorhídrico (HF). Son empleadas en la fabricación de pastas dentales y otros insumos odontológicos. Ejemplos: NaF, KF, LiF, CaF 2. Sulfatos (SO42-). Aniones que forman parte de sales o ésteres obtenidas a partir del ácido.
¿Qué es un enlace iónico? Características, propiedades y ejemplos Plataformasinc.es
Compuestos Covalentes. Gases, líquidos, o sólidos (hechos de moléculas) Bajos Puntos de Ebullición y Fusión. Pobres conductores eléctricos en todas las fases. Muchos son solubles en líquidos no polares pero no en agua. A partir de las posiciones de los componentes en la tabla periódica, se puede anticipar algunas cosas sobre los enlaces.
Realizar 7 ejemplos de enlace interatómicos (3 iónicos, 2 covalentes polares y 2 covalentes no

Características del enlace iónico. El enlace iónico -también conocido como enlace electrovalente- es un tipo de unión química en el que existe una atracción. Puntos de fusión y ebullición altos. Los puntos de fusión y ebullición de los compuestos iónicos son especialmente altos debido a sus fuertes interacciones electrostáticas.
Enlace químico qué es, definición, tipos, cómo se forman, ejemplos
Por ejemplo, la fórmula del óxido de aluminio, Al 2 O 3, indica que este compuesto iónico contiene dos cationes de aluminio, Al 3+, por cada tres aniones de óxido, O 2− [así, (2 × × +3) + (3 × × -2) = 0]. Sin embargo, es importante señalar que la fórmula de un compuesto iónico no representa la disposición física de sus iones.
Punto de fusión y punto de ebullición YouTube

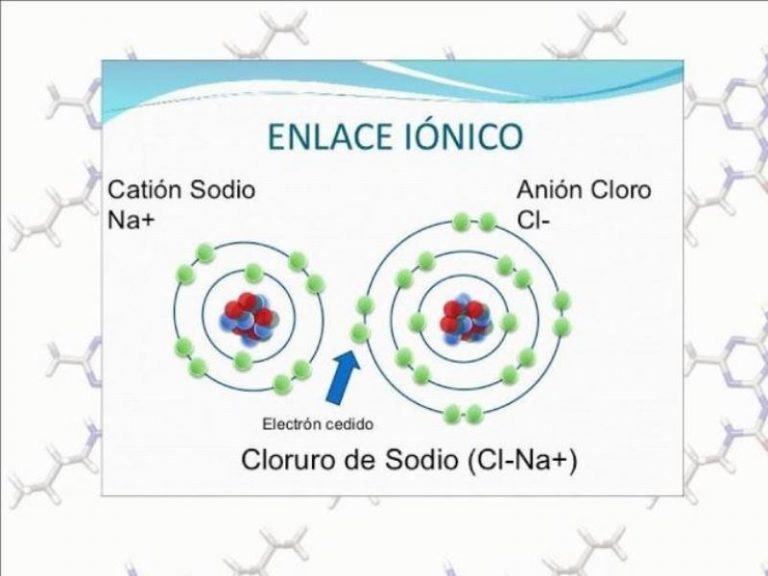
Transcripción del video. los enlaces iónicos son los enlaces que mantienen unidos a los compuestos iónicos es decir que mantienen juntos a los cationes y añón es un ejemplo muy común de un compuesto que se mantiene unido por medio de un enlace iónico es el cloruro de sodio también conocido como sal de mesa aquí tenemos una imagen.